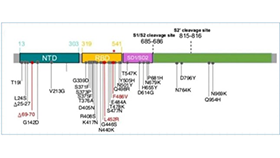
大肠埃希菌(Escherichia coli,E.coli)作为人体肠道正常菌群,属于革兰阴性杆菌,对人体健康具有重要生理功能。然而,随着抗菌药物的广泛使用及基因水平转移的发生,部分大肠埃希菌进化为碳青霉烯耐药菌株(CREC),成为临床感染领域的重要威胁[1]。
肠道共生菌的两面性:
从有益共生到致命感染
E.coli作为人体肠道正常菌群,参与维生素B族、K族的合成及肠道微生态平衡维持,但在肠道屏障受损、免疫功能低下或菌株获得毒力基因时,可引发尿路感染、腹腔感染、血流感染等疾病[2]。近年来,抗菌药物选择压力与基因水平转移共同驱动大肠埃希菌的致病性进化,尤其是碳青霉烯耐药高毒力菌株(hypervirulent carbapenem-resistant strains hv-CREC)的出现,打破了“共生菌”的定位。碳青霉烯类药物作为治疗严重革兰氏阴性菌感染的最后防线,其耐药性的产生使hv-CREC感染面临用药困难的窘境,高毒力表型则会进一步加剧不良临床预后。
CREC的进化机制:
耐药与毒力叠加
CREC 的进化机制:耐药与毒力叠加
CREC的耐药性主要源于碳青霉烯酶的获得,其中blaNDM是最常见的耐药基因型,通过质粒介导在菌株间快速传播。研究显示:我国大肠埃希菌临床分离株中,80.7%的CREC携带 blaNDM-5基因,部分菌株亦可检出 blaKPC、blaOXA 等碳青霉烯酶基因。此类基因可水解包括碳青霉烯类在内的多种β-内酰胺类抗生素,进而介导菌株对临床常用抗菌药物产生耐药性[3]。
高毒力进化:基因重组与毒力基因整合
CREC的高毒力特征源于基因组重组与毒力基因的整合。我国学者对653株 hv-CREC的研究发现,ST167 型菌株中的 KpnK48 亚克隆是流行的主要驱动因素,该亚克隆通过获得492kb的重组基因组区域,获得了与hv-CRKP ST11-K64克隆同源的基因簇。该区域包含K48荚膜基因、ICEKp4毒力岛(携带 yersiniabactin 铁载体系统)、parDE毒素 - 抗毒素系统等,显著增强了菌株的免疫逃逸能力、铁离子获取能力及抗生素耐受性[2]。
序列型(ST)167、ST410、ST617和ST361共同占CREC分离株的53.8%(351/653),其中ST167在2017年后显著增加。KpnK48克隆株从广泛存在的NDM-IncX3 质粒转变为大肠杆菌常见的NDM-IncF质粒,进一步增强了其致病性和传播性。目前,KpnK48亚克隆已在我国15个省份的43家医院传播,且存在人畜共患传播风险[2,4]。
CREC成为全球公共卫生的严峻挑战
全球死亡率与经济负担
2021年全球约471万人的死亡与细菌耐药相关,其中114万人直接归因于细菌耐药感染。CREC 感染作为严重耐药菌感染类型,可导致患者住院时间延长(中位数25天)、治疗费用增加,且死亡率显著高于敏感菌感染。在血液病患者中,CREC血流感染的死亡率虽低于CRKP感染(18% vs 44%),但仍显著高于其他细菌感染[2,3]。
我国的流行特征
CHINET2025年上半年监测数据显示:我国临床分离E.coli中,对亚胺培南和美罗培南的耐药率分别为2.2%和2.3%,且近年来CREC在二、三级医院检出率呈缓慢上升趋势。儿童医院CREC检出率(3.0%)高于综合医院[4],我国 CREC 流行存在显著地域差异:华中地区检出率最高(7.04%),华北地区次之(6.16%),西南地区有数据医院显示检出率为1.27%,三级医院及 ICU 等重症科室检出率显著更高,ICU可达 9%~10%[5]。耐药机制方面:CREC以产金属β-内酰胺酶(MBL)为主,2024年占比达78.4%,以NDM-1、NDM-5 型最为常见,次要耐药机制为产KPC型(10%~15%)与OXA-48型酶(5%),同时携带多碳青霉烯酶基因的菌株亦有出现 [5,6]。
CREC感染的高危人群:
免疫脆弱与医疗暴露并存
免疫功能低下人群
①血液病患者、接受化疗、造血干细胞移植或免疫抑制治疗者。研究显示,血液病患者中CREC血流感染的30天死亡率达18%,其中合并粒细胞缺乏、多部位感染的患者风险更高。
②老年人、儿童(尤其是新生儿)、免疫缺陷病患者,也因免疫屏障薄弱,易发生CREC感染。
医疗相关暴露人群
①ICU患者、接受侵入性操作(如机械通气、中心静脉置管、导尿)或长期使用广谱抗生素的患者,由于肠道屏障受损及耐药菌定植风险增加,成为CREC感染的重点防控人群。
②我国一项多中心流行病学研究显示:ICU分离的E.coli对多数抗菌药物的耐药率显著高于非ICU科室。ICU 分离株对亚胺培南(耐药率3.7%vs非ICU科室 1.1%-2.5%)、美罗培南(4.1%vs1.1%-3.0%)、头孢他啶(32.3%vs21.1%-30.2%)等多种抗菌药物的耐药率均高于门诊、急诊、内科、外科等非 ICU 科室[4]。
特殊生理与疾病状态人群
①女性由于泌尿系统生理结构特点,泌尿系感染风险显著高于男性,而CREC引起的泌尿系感染易进展为血流感染。
②合并糖尿病、慢性肾病、腹腔基础疾病的患者,因局部微环境改变和免疫功能紊乱,增加了CREC感染的发病风险。
从经验治疗到靶向干预
遏制细菌耐药,精准诊断对于CREC感染的防控与治疗至关重要。通过微生物鉴定技术区分CREC与其他碳青霉烯耐药菌(如CRKP),可依据菌株药敏差异(如CREC对替加环素敏感性更高)优化治疗方案;借助核酸快速检测技术,明确致病菌和耐药基因型能有效避免经验治疗盲目性,为携带不同耐药基因的菌株匹配准确治疗药物,显著提升治疗成功率。还能及时识别流行风险,为医院感染防控提供科学依据[2,3]。
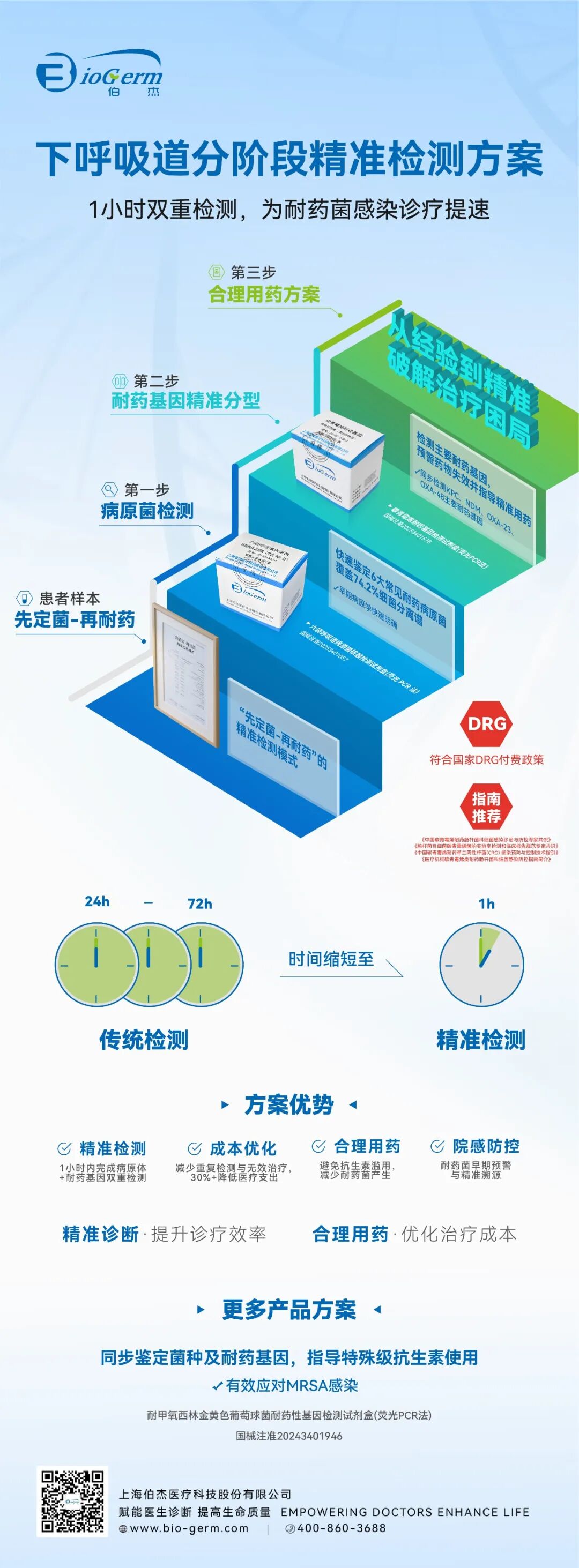
上海伯杰医疗的下呼吸道六项细菌检测试剂,涵盖肺炎链球菌、肺炎克雷伯菌、大肠埃希菌、铜绿假单胞菌、鲍曼不动杆菌及流感嗜血杆菌,另外伯杰医疗自主研发的碳青霉烯耐药核酸检测试剂盒可精准检测KPC、NDM、OXA-23、OXA-48 四类常见基因型,精准契合遏制细菌耐药的临床需求。前者覆盖下呼吸道高发致病菌,后者同步锁定NDM、KPC等耐药基因,实现“病原菌+耐药基因”一小时快速出结果。为患者筛查与明确病因提供高效手段,切断传播链、减少碳青霉烯类药物滥用。这不仅为临床快速筛查、明确病因提供了高效可靠的手段,更有助于合理用药、减少碳青霉烯类药物滥用,为切断耐药菌传播、遏制细菌耐药趋势提供了坚实的技术支撑。
文字丨医学部
编辑丨品牌宣传部
图片丨来源于伯杰医疗














.jpg)