2022病原检测与传染病监测学术交流大会于7月9日-10日成功召开。本次会议邀请了传染病防控、临床诊疗和检测技术等领域的国内知名专家学者,共话病原检测和传染病监测的前沿技术,分析和总结传染病防控体系国内外的发展现状和趋势,为传染病的防控事业贡献绵力。
本次,伯杰医疗有幸邀请到江西省疾病预防控制中心疾病控制检验所副所长李健雄作为讲者,在监测干预分会会议上为我们分享了《奥密克戎流行形势下新型冠状病毒检测新需求》。
新型冠状病毒肺炎防控方案(第九版)指出:"现有研究提示,奥密克戎变异株的平均潜伏期缩短,多为2-4天,其传播能力更强,传播速度更快,感染剂量更低,致病力减弱,具有更强的免疫逃逸能力,已经成为我国境外输入和本土疫情的优势流行株。
奥密克戎变异株流行的情况下,我们对新型冠状病毒检测又有哪些新的需求呢?李健雄所长的报告围绕:奥密克戎的流行趋势,奥密克戎流行形势下对检验的新需求两个方面重点展开。

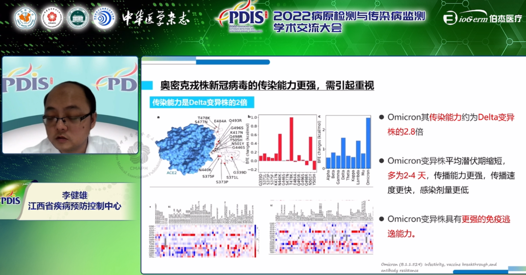
新冠病毒“变异”持续存在,并且在全球传播。其中,奥密克戎株新型冠状病毒的传染能力更强。主要表现为:
奥密克戎变异株的传染能力约为德尔塔变异株的2.8倍;
奥密克戎变异株平均潜伏期缩短,多为2-4天,传播能力更强,传播速度更快,感染剂量更低;
奥密克戎变异株具有更强的免疫逃逸能力。
目前,奥密克戎已成为全球流通的主要毒株,而最近出现的奥密克戎BA.4、BA.5亚型也已经成为流行趋势上升最快的亚型。

左右滑动查看
常规核酸检测速度:对于愿检尽检人群,由最开始24小时出报告变为6小时出报告;
大规模筛查核酸检测速度:从2020年500万人口城市5-7天完成全员检测变为今年1000万人以上人口城市24小时完成划定范围区域的核酸检测。且最新的第九版新冠疫情防控方案要求在疫情存在扩散风险时,需每日开展一次全员核酸检测。
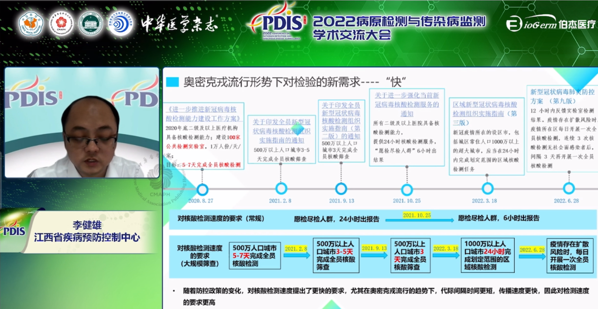
李健雄所长提出可以从以下几个方面提高检测速度:
增加仪器和人员;
检测试剂和检测仪器的更新换代:
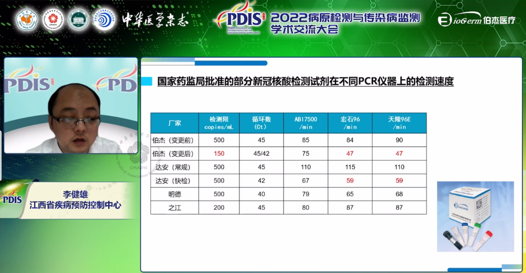
(1) 优化核酸提取仪和PCR检测仪:选择运行时间更短或检测通量更大的仪器设备,从而提高单次核酸检测能力,提高检测速度。
(2) 优化检测试剂:在不降低检测灵敏度的情况下,优化扩增程序,缩短新冠核酸检测试剂的时间,提高检测速度。如伯杰变更后的新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法)可在47分钟内完成检测,且灵敏度为150copies/mL。
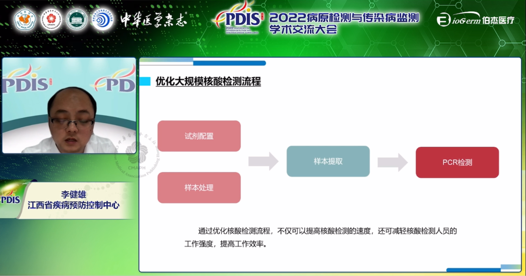
优化大规模核酸检测流程:
通过优化核酸检测流程,不仅可以提高核酸检测的速度,还可以减轻核酸检测人员的工作强度,提高工作效率。李健雄所长提出:大规模核酸检测流程可采用流水线的工作模式,分为试剂配置,样本处理,样本提取和PCR检测四个组。每个组的人员分工明确,保证检测流程顺利进行,可有效提高核酸检测速度。

左右滑动查看
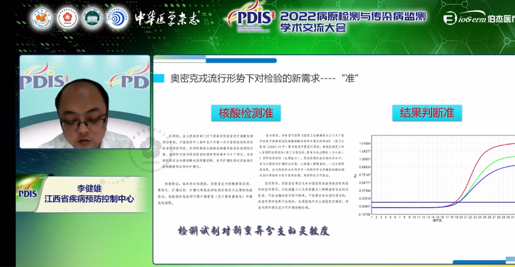
检测结果准:2022年1月15日国家卫健委颁发的《新冠病毒核酸20合1混采检测技术规范》指出,20合1混采检测技术可大幅度提高检测效率,更加适用于大规模人群核酸筛查工作。而混采相比较单采而言,为保证弱阳性样本的检出,对核酸检测试剂的灵敏度要求则更高,其标准由原来的1000copies/mL变为500copies/mL。
结果判读准:最新版的新冠疫情防控方案对核酸检测结果(CT)值的判断提出了更高的要求。国内有关研究显示,处于恢复期的感染者在核酸Ct值≥35时,样本中未能分离出病毒,密切接触者未发现被感染的情况。第九版诊疗方案中更新了解除隔离管理的标准,选择与第九版诊疗方案中描述的新冠核酸检测结果判读界限值一致的试剂,可更加高效、快速地完成新冠核酸检测结果的判读和相关人员隔离/出院的判定。
注:第九版诊疗方案中对于解除隔离管理标准规定:轻型病例连续两次新型冠状病毒核酸检测N基因和ORF基因Ct值均≥35(荧光定量PCR方法,界限值为40,采样时间至少间隔24小时),或连续两次新型冠状病毒核酸检测阴性(荧光定量PCR方法,界限值低于35,采样时间至少间隔24小时),可解除隔离管理。
近几版新冠疫情防控方案明确要求要对核酸检测Ct值≤32的本土疫情中的首发或早期病例、与早期病例有流行病学关联的关键病例、感染来源不明的本土病例、境外输入病例、入境物品及相关环境阳性标本、疫苗接种后核酸检测阳性者标本进行测序。
在未来,除了加强人员培训,也希望有更先进的设备使得全基因组测序操作更加简单,有更方便的分析软件,取得更准确的测序数据。
四. 伯杰新冠核酸试剂全新升级:传承稳定性,追求新体验
《新型冠状病毒肺炎防控方案(第八版)》建议选用高敏感性的试剂(检测限≤500拷贝/mL),但随着《新冠病毒核酸20合1混采检测技术规范》的发布,对核酸检测试剂的灵敏度要求越来越高。
在保证试剂特异性的前提下,如何提升灵敏度成为考验新冠核酸检测企业的一大难题,伯杰医疗研发团队从扩增反应体系入手,通过增加上样量提升起始模板量,然后对体系进行优化配置,使得镁离子等盐类维持在了更合适的浓度,从而降低非特异扩增,并将灵敏度从500copies/mL提升至150copies/mL。
扩增时间再缩短, 最快35分钟
检测时间的制约因素往往来自适配PCR仪器的性能,伯杰医疗根据不同品牌的PCR仪器适配性优化了扩增程序,针对逆转录、预变性、退火/延伸/检测荧光等步骤进行了温度和时间上的优化,最快可在35分钟内完成扩增检测全过程。
拓展能力提升,兼容更多平台
伯杰医疗新款的新冠核酸检测试剂盒适配ABI 7500、宏石SLAN-96S、安誉AGS-8830等荧光定量PCR仪,试剂的稳定性也得到了进一步的提升。伯杰医疗对10余种PCR仪器品牌的适配性能进行了充分验证,适配性能更优,根据不同PCR仪器升降温速度,反应时间可进一步缩短!
上海伯杰医疗科技股份有限公司是一家致力于感染性病原体分子诊断试剂研发和应用,深耕于多重荧光PCR诊断试剂和痕量病毒二代测序试剂及相关服务的国家高新技术企业。公司围绕感染性病原体这一主线,从诊断试剂、诊断仪器、测序服务和医检所服务等多个面提供全套解决方案。公司秉承“勇于创新,质量为先”的方针,为医疗机构、疾控公卫、高校科研等合作伙伴提供优质产品与服务。

全国客服电话:400-860-3688














.jpg)